台灣自產疫苗最快明年冬季上市 人體試驗8月展開

國光生技董事長詹啟賢強調,因應新冠肺炎,疫苗開發動物與人體試驗將加快進行,希望明年冬季量產。(攝影/陳敬哲)
文:陳敬哲(NOW健康)
台灣自產中共肺炎疫苗,預計明年冬季量產!今(6)日國光生技對外公布,已經成功生產中共肺炎候選疫苗,第1期人體試驗將在8月展開,第2期與第3期人體試驗預計將在明年第1季開啟,待安全性與有效性順利確定後,明年下半就能生產批量出貨,國光強調技術台灣完全擁有,產出疫苗一定以台灣優先。
實驗鼠疫苗抗體血清 有效抑制病毒培養
國光生技與台灣大學病毒實驗室張淑媛教授合作,確認候選疫苗有效性,張淑媛表示,將候選疫苗注入實驗老鼠,當抗體生成後藉由血清分離,將抗體與病毒同時放置培養皿,發現候選疫苗產製抗體,能有效抑制病毒,並且一定程度能稀釋抗體,也能夠讓病毒失去感染力,證實候選疫苗有效性。
國光生技董事長詹啟賢進一步解釋,如果在流感疫苗上,疫苗抑制率能達80%,就能稱作有效疫苗,此次中共肺炎候選疫苗中,抗體血清稀釋320倍,病毒抑制率高達100%,稀釋到1,280倍也能有80%抑制率,當抗體血清稀釋到1萬倍左右,培養皿才明顯可以培養出病毒,顯示疫苗產製抗體非常有效。
國光1月開始準備 強調有效比早實驗重要 詹啟賢強調,國光生技今年1月就開始準備,各國疫苗生產技術不同,事前準備工作也就不同,疫苗生產出來最重要仍然要評估安全與有效,事前準備工作越足,後續遇到的困難就有可能減少。意味著國外雖然部分研究機構開始人體試驗,但也不一定能確定最終成果。
針對研發時程詹啟賢也說,中共肺炎疫苗動物實驗,預計今年5月就開始10月完成,但只要確認安全與有效,在8月就會先執行第1期臨床試驗,預估明(2021)年第1季完成,緊接著就同步執行第2期與第3期人體測試,同時間也檢測GMP量產效能,如果一切非常順利,預計明年冬季就可量產疫苗。
國光申請緊急使用授權 各項實驗可同時進行
詹啟賢特別指出,一般疫苗研發,每一次試驗都幾乎不會時間重疊,例如動物實驗做完,才會接著第1期人體試驗,完成再接著第2期人體試驗等,否則動物實驗最終結果失敗,第1期人體試驗也就作廢;但此次中共肺炎疫情特殊,希望疫苗安全有效,又希望能盡快量產,因此願意承擔試驗失敗風險。
詹啟賢也提到,此次疫苗研發,先前已經與台灣食藥署(TFDA)與醫藥品查驗中心(CDE)討論,怎麼樣用安全與有效為前提,用緊急使用授權(EUA)方案提早開始人體試驗,並且CDE已經同意將國光的中共肺炎疫苗開發案,列為專案諮詢輔導案件,計畫向前推進。
國光強調 生產疫苗不影響流感疫苗
詹啟賢提醒,如果冬季容易引起中共肺炎疫情,明年冬季可以同時施打中共肺炎與流感疫苗。同時也補充說明,中共肺炎疫苗產線與流感疫苗不同,國光不會因生產中共肺炎疫苗而減少流感疫苗的生產量,兩個疫苗生產方式也不同,目前國光正在擴增產線與廠房,希望能帶起疫苗產製量,讓全體台灣民眾都能施打。
相關新聞
-

中國疫情嚴峻 多地猝死暴增
2024-04-06 19:38:56中國大陸的疫情從未消失。日前,多地民眾反映,從去年底至今,身邊許多人出現染疫重症,猝死率暴增。由於太多人死,大家都不願意去殯儀館,也不開追悼會了。
-

知情人:中共隱瞞疫情 要求銷毀所有新冠資料
2024-03-01 21:21:23中國新年後,各地疫情持續升溫,中共一貫隱瞞疫情真相。 近日,有知情人士透露,中共已要求全國的醫療系統,銷毀所有的中共病毒Covid-19新冠相關資料。
-

中國「甲流」引爆心肌炎 症狀似新冠 死亡率超高
2023-03-17 21:11:04在這場當局宣稱的所謂「甲流」浪潮下,不少患者出現心肌炎症狀,民眾懷疑,這些症狀,和新冠類似,可能還是新冠病毒導致的。
-

本土+382 金門2例陰轉陽 境外+149
2022-04-07 14:46:21中央流行疫情指揮中心今(7)日公布,國內新增531例COVID-19確定病例,分別為382例本土個案及149例境外移入,其中78例為航班落地採檢陽性;另確診個案無新增死亡。
-

台本土+216今年首破200 新北91、基隆33
2022-04-05 14:31:22中央流行疫情指揮中心今(5)日公布,國內新增281例COVID-19確定病例,分別為216例本土個案及65例境外移入,其中28例為航班落地採檢陽性;另確診個案無新增死亡。
-

初三本土+22例!中國返台過年1家4口確診
2022-02-04 22:19:14中央流行疫情指揮中心今(3)日公布國內新增56例COVID-19確定病例,分別為22例本土個案及34例境外移入(10例為航班落地採檢陽性);另確診個案中無新增死亡。
-

本土+82、境外+48 亞旭桃園廠群聚累計70人
2022-01-22 15:49:23今(22)日中央流行疫情指揮中心公布,國內新增130例COVID-19確定病例,分別為82例本土個案及48例境外移入;另確診個案中無新增死亡。
-
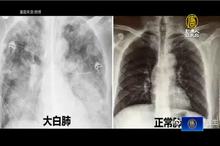
中共與天鬥清零失敗 陸網友轟「白肺心肌」
2023-01-03 16:38:54中共長達三年的清零封控失敗,現在疫情大爆發,出現「白肺」與「心肌炎」症狀的患者不斷蔓延至各個年齡層,有網友發文,家裡剛出生5天的新生兒,感染後遭醫院下病危通知書,右肺1/3出現白肺。由於中國本輪疫情中出現了大量「白肺」和「心肌炎」患者,中國網友更是創出了「白肺心肌」一詞,諷刺中共戰天鬥地的無效三年「清零」。目前,國際持續要求中共公布真實疫情數據,中國醫衛專家張文宏指出,過年期間,中國染疫比率可能高達80%,代表中國14億人口將有超過11億人染疫。
-

中共寧見疫情失控 拒絕美國、德國援助疫苗
2022-12-22 20:37:31中國近期疫情爆發嚴重,美國和德國政府紛紛對此表態,願意提供疫苗來協助控制疫情,然而中共寧願看人民陷於水深火熱,也不願意接受兩國的提議。
-

北上廣現染疫潮醫院病患爆增 官方罕見警告
2023-04-29 20:34:26中國長假在即,中共突然警告民眾,有染疫風險,引發各界擔憂,認為中共很可能再一次為保經濟而掩蓋疫情,從而導致長假出遊的人們,將病毒散播到全國各地。
-

本土+15 桃園9例最多 境外移入+33 美國最多
2022-01-29 15:09:03今(29)日中央流行疫情指揮中心公布,國內新增15例本土個案及33例境外移入;另確診個案中無新增死亡。
-

本土+13 境外移入+25 桃園增加3例不明感染源
2022-01-25 15:12:37今(1/25)中央流行疫情指揮中心宣布,新增13例本土、25例境外移入,死亡個案則未增加。新增本土個案為4例男性、9例女性,年齡介於未滿5歲至70多歲。
-

本土+15例 境外移入+36例 新年期間維持二級警戒標準
2022-01-24 15:27:42今(24)日中央流行疫情指揮中心公布,國內新增51例COVID-19確定病例,分別為15例本土個案及36例境外移入;另確診個案中無新增死亡。
-

+37例本土 11例陰轉陽 26例不明感染源 46例境外移入
2022-02-10 15:03:47今(10)日中央流行疫情指揮中心公布,國內新增83例COVID-19確定病例,分別為37例本土個案及46例境外移入,15例為航班落地採檢陽性;另確診個案中無新增死亡。
-

中國偷偷強推第4針?!拒絕者禁出門甚至收押
2023-04-04 20:20:57近日,中共御用專家鐘南山的一番話,令人擔憂,疫情再度爆發,不是空穴來風。還有民眾透露,山東正在偷偷強推第4針疫苗,如果拒絕,被禁止出門,甚至「收押」。
-

+16例本土 44例境外移入 7例落地採檢陽性
2022-02-01 15:05:48今(1)日中央流行疫情指揮中心公布,國內新增16例本土個案及44例境外移入,其中7例為航班落地採檢陽性;另確診個案中無新增死亡。
-

本土+281 全台17縣市確診 境外+78
2022-04-06 15:03:09中央流行疫情指揮中心今(6)日公布,國內新增359例COVID-19確定病例,分別為281例本土個案及78例境外移入,其中27例為航班落地採檢陽性;另確診個案無新增死亡。
-
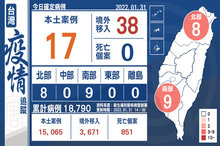
+17例本土 38例境外移入 美國最多
2022-01-31 16:33:40今(31)日中央流行疫情指揮中心公布,國內新增17例本土個案及38例境外移入(20例為航班落地採檢陽性);另確診個案中無新增死亡。
-

台本土+133 境外+142 雙北、桃園確診數多
2022-04-04 14:52:39中央流行疫情指揮中心今(4)日公布,國內新增275例COVID-19確定病例,分別為133例本土個案及142例境外移入,其中68例為航班落地採檢陽性;另確診個案無新增死亡。
-

台本土+104 境外+132 桃園電商群聚新增22例
2022-04-01 14:45:34中央流行疫情指揮中心今(1)日公布,國內新增236例COVID-19確定病例,分別為104例本土個案及132例境外移入,其中75例為航班落地採檢陽性;另確診個案無新增死亡。






 財經趨勢4.0
財經趨勢4.0 新聞大破解
新聞大破解 新唐人財經新聞
新唐人財經新聞 選戰大透視
選戰大透視 遇見新聞
遇見新聞 老外看中國、老外看台灣
老外看中國、老外看台灣 美麗心台灣
美麗心台灣 田美女奉茶實客
田美女奉茶實客 廚娘香Q秀
廚娘香Q秀 大千世界
大千世界 1000步的繽紛台灣
1000步的繽紛台灣 好樣!Formosa
好樣!Formosa 健康1+1
健康1+1 談古論今話中醫
談古論今話中醫 我的音樂想想
我的音樂想想 胡乃文開講
胡乃文開講 她健康She Health
她健康She Health 天庭小子-小乾坤
天庭小子-小乾坤 總統教育獎
總統教育獎 全國孝行獎
全國孝行獎 健談交流
健談交流 悠遊字在
悠遊字在 傳奇時代
傳奇時代 音樂大賽特別節目
音樂大賽特別節目










































