高端疫苗研發將在越南收案 食藥署:國內需有千人

高端疫苗研發將在越南收案 食藥署:國內需有千人(資料畫面)
文:陳敬哲(NOW健康)
台灣疫苗業者高端,今(2)日在記者會對外宣布,與越南衛生部轄下國家衛生暨流行病學研究所(NIHE)合作研發中共肺炎疫苗,主要目的在加快臨床人體試驗收速度,衛福部食藥署表示,符合緊急授權第2階段臨床試驗,必須有3,000名受試者,當中台灣受試者必須有1,000名以上。
媒體報導高端對外表示,今年9月已經在台灣展開第1期臨床實驗,第2期臨床實驗將納入越南與其他地區收案,可以加速2期臨床實驗時間,有助於更快取得台灣與其他地區疫苗緊急授權上市;高端補充,越南是東協重要成員國,人口將近1億,高端與越南合作,可以提供當地防疫所需,也是進入東協市場佈局。
食藥署藥品組副組長吳明美接受媒體採訪時表示,原則上符合緊急授權條件,第2期臨床實驗必須有3,000名受試者,同時當中也要有1,000名台灣受試者,至於其他2,000件與國外合作個案,要用哪一個國家受試者,食藥署會由「第2期臨床試驗申請書」中規定,確認研發業者是否符合規範。
根據媒體報導,中共肺炎疫苗國內研發業者,目前國光、聯亞、高端都已經在第1期臨床實驗階段,食藥署在10月14日首度召開專家會議討論,制訂第2期臨床試驗需要資料與緊急授權標準,也參考美國食藥局的緊急授權指引,確定總受試者要有3,000人,而國內疫苗受試者必須至少有1,000人,才能啟動緊急授權。
相關新聞
-

高端通過保護效益審查 指揮中心釋疑三期試驗
2022-11-04 22:30:40再來看到,食藥署審查高端遞交疫苗保護效益,昨天(3日)晚上宣布,高端疫苗有良好保護效益。高端續保留EUA緊急使用權資格。審議資料包括疫苗保護效益評估報告、國內全人口大數據資料,以及國內臨床資料庫分析報告。
-

高端疫苗技轉授權WHO 生產研發基地首曝光!
2023-09-18 20:03:54台灣的國產疫苗研發實力受到國際肯定。高端COVID-19疫苗技轉授權給世界衛生組織(WHO),創下全球首例。研發十年的腸病毒71型疫苗,也已經上市。這些疫苗的生產研發基地,就在高端疫苗的新竹竹北廠區。首次對外曝光,帶您了解。
-

世衛獲高端COVID-19疫苗技轉授權
2023-08-30 08:06:50世界衛生組織旗下COVID-19技術近用聯盟(C-TAP)和藥品專利聯盟(MPP),昨天分別宣布,取得台灣疫苗廠高端COVID-19疫苗技轉許可協議,創下全球疫苗首例,高端指出,未來C-TAP及MPP如果再授權予第三方,高端可收取合理且被授權方可負擔之授權金。
-

中國「甲流」引爆心肌炎 症狀似新冠 死亡率超高
2023-03-17 21:11:04在這場當局宣稱的所謂「甲流」浪潮下,不少患者出現心肌炎症狀,民眾懷疑,這些症狀,和新冠類似,可能還是新冠病毒導致的。
-

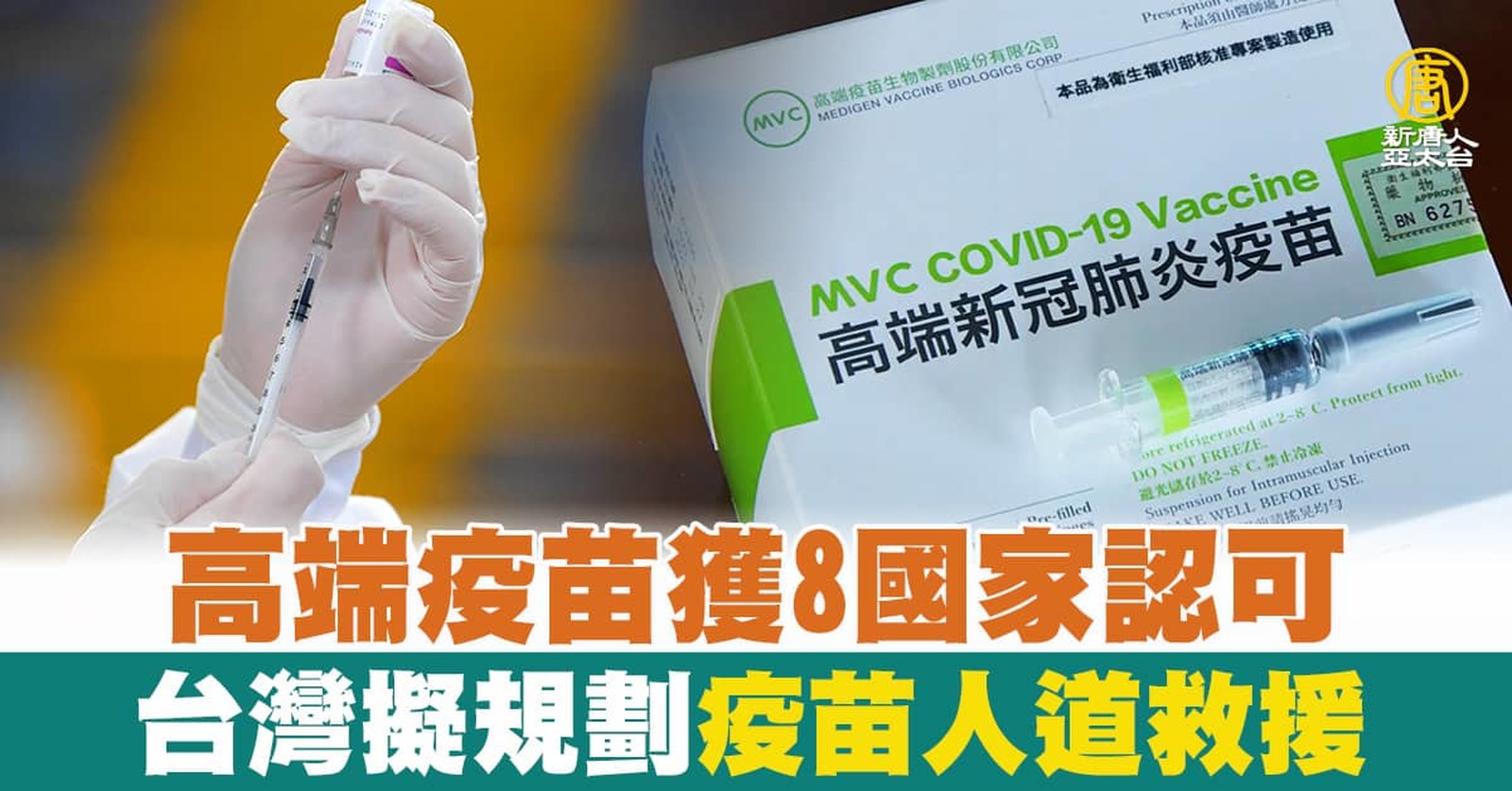
高端疫苗獲8國家認可 台灣擬規劃疫苗人道救援
2022-02-16 16:19:16高端COVID-19疫苗昨天獲得巴拉圭政府EUA,指揮中心指揮官陳時中今天表示,目前全球共8國承認高端疫苗,台灣剩餘300萬劑除供國內使用,也會規劃作人道救援。
-

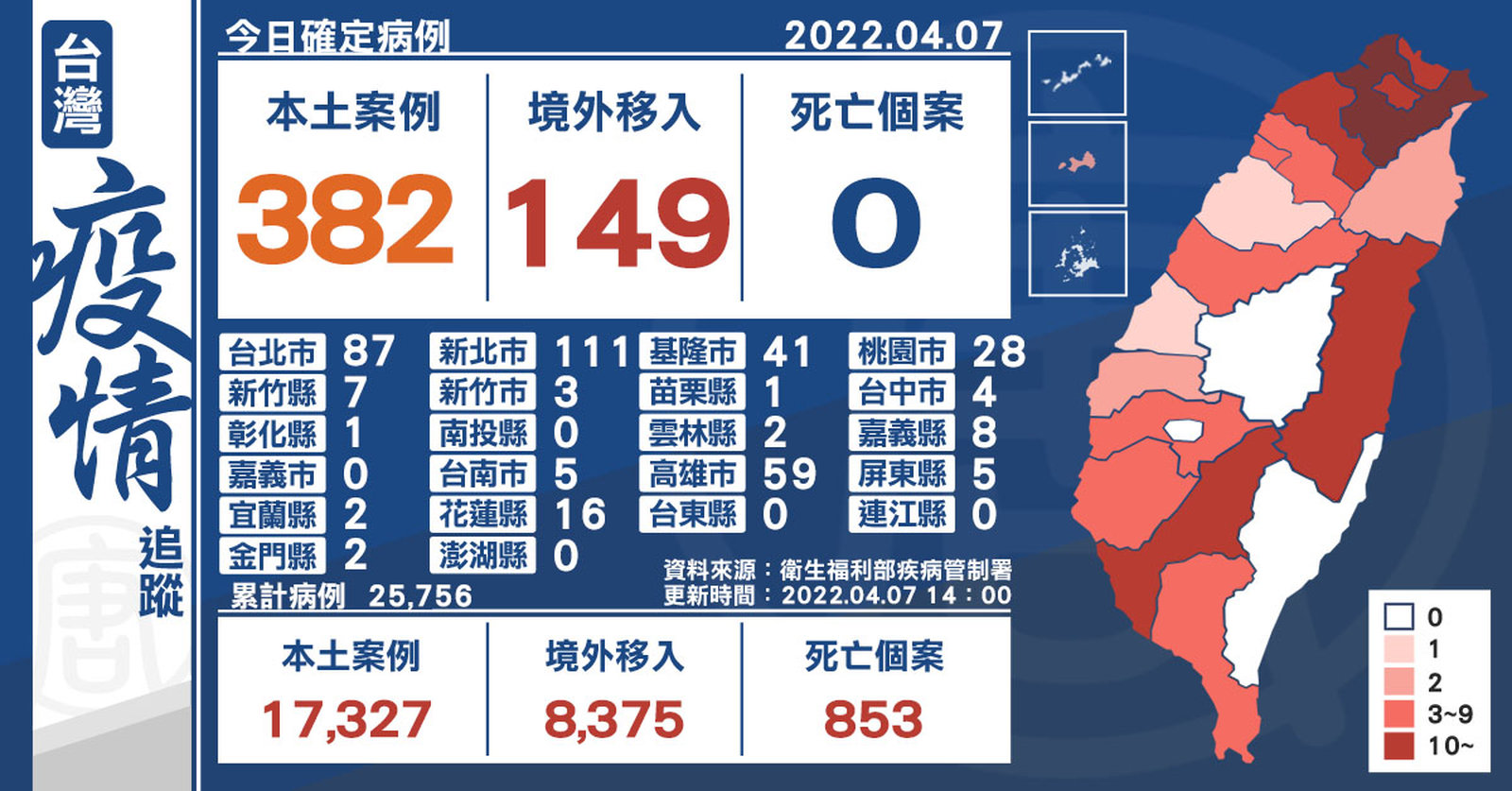
本土+382 金門2例陰轉陽 境外+149
2022-04-07 14:46:21中央流行疫情指揮中心今(7)日公布,國內新增531例COVID-19確定病例,分別為382例本土個案及149例境外移入,其中78例為航班落地採檢陽性;另確診個案無新增死亡。
-

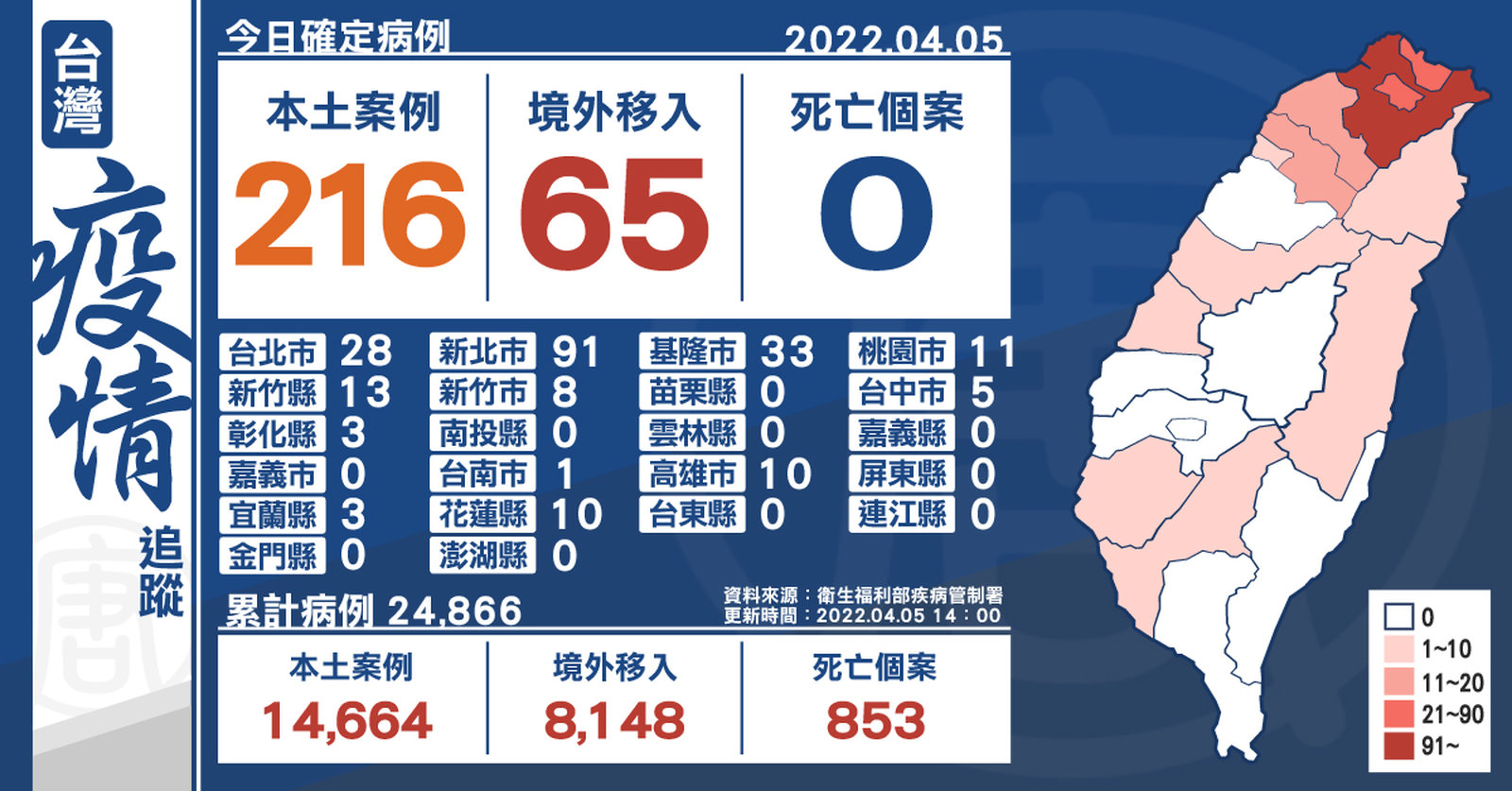
台本土+216今年首破200 新北91、基隆33
2022-04-05 14:31:22中央流行疫情指揮中心今(5)日公布,國內新增281例COVID-19確定病例,分別為216例本土個案及65例境外移入,其中28例為航班落地採檢陽性;另確診個案無新增死亡。
-

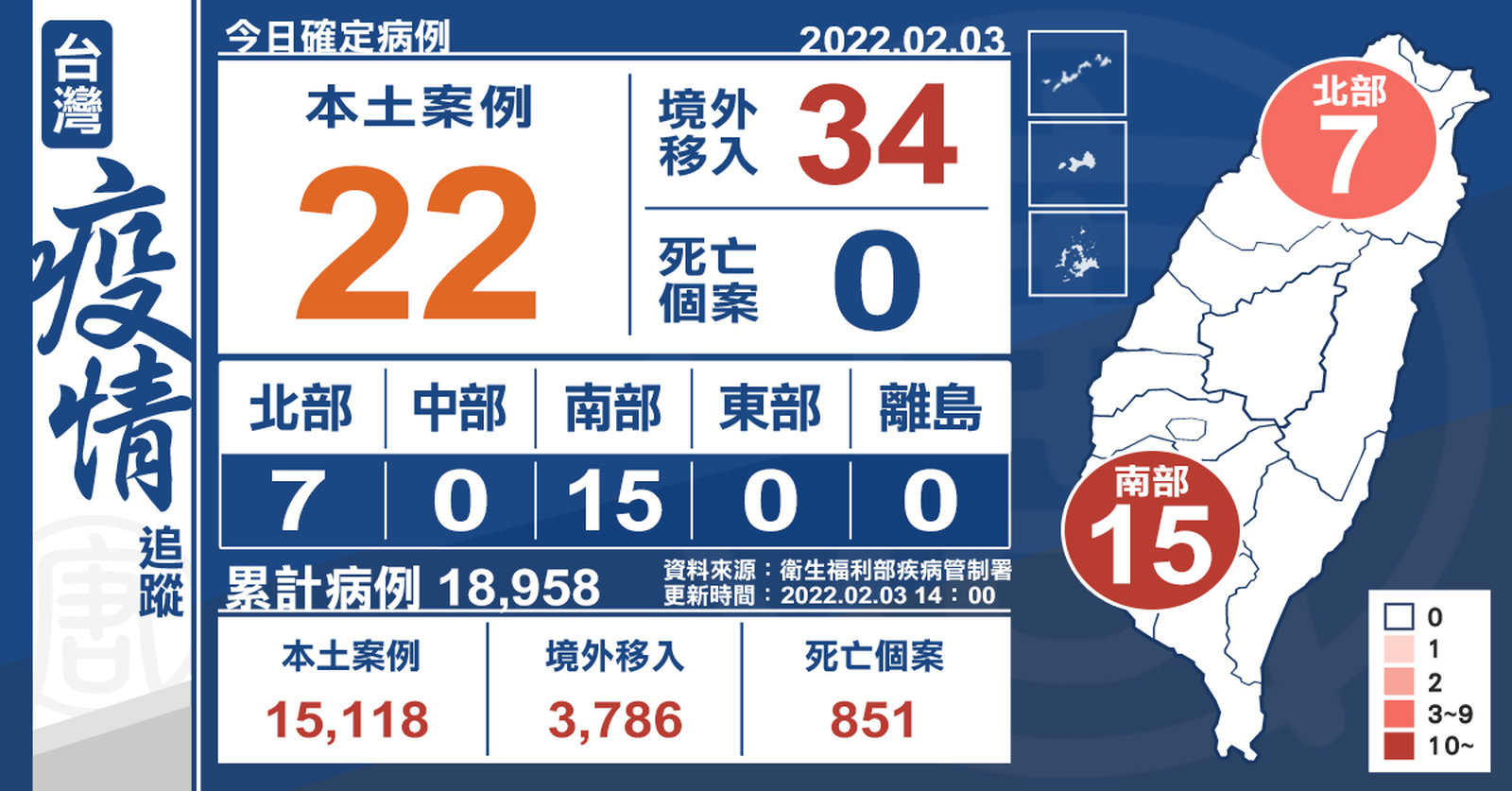
初三本土+22例!中國返台過年1家4口確診
2022-02-04 22:19:14中央流行疫情指揮中心今(3)日公布國內新增56例COVID-19確定病例,分別為22例本土個案及34例境外移入(10例為航班落地採檢陽性);另確診個案中無新增死亡。
-

中共寧見疫情失控 拒絕美國、德國援助疫苗
2022-12-22 20:37:31中國近期疫情爆發嚴重,美國和德國政府紛紛對此表態,願意提供疫苗來協助控制疫情,然而中共寧願看人民陷於水深火熱,也不願意接受兩國的提議。
-

北上廣現染疫潮醫院病患爆增 官方罕見警告
2023-04-29 20:34:26中國長假在即,中共突然警告民眾,有染疫風險,引發各界擔憂,認為中共很可能再一次為保經濟而掩蓋疫情,從而導致長假出遊的人們,將病毒散播到全國各地。
-

高端疫苗巴拉圭三期解盲達標 獲EUA
2022-02-15 16:30:05全球超過4億1千萬人確診染疫,超過582萬人病逝。台灣國產疫苗,高端疫苗宣布,在巴拉圭三期疫苗的臨床解盲結果,安全性、耐受性和高免疫原性等方面符合要求,巴拉圭在今天核准緊急使用授權(EUA);高端表示,同時也將跟其他國家法規單位溝通,申請EUA。高端表示,當地數據顯示,中和抗體效價達對照組AZ疫苗的3.7倍,與台灣做的數據差異不大;此項試驗總計在巴拉圭收納1128名受試者,並有934名受試者完成兩劑疫苗接種。另外,高端獲WHO主導與出資,在菲律賓、哥倫比亞及馬利共和國,進行傳統安慰劑對照的疫苗有效性第三期
-

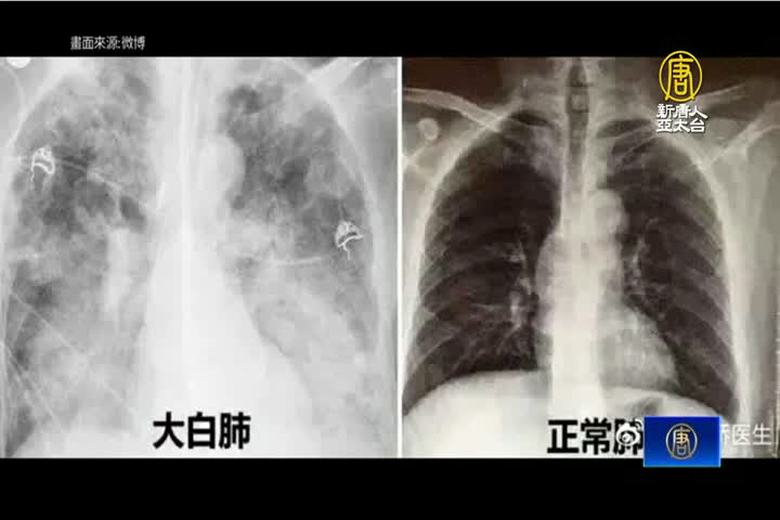
中共與天鬥清零失敗 陸網友轟「白肺心肌」
2023-01-03 16:38:54中共長達三年的清零封控失敗,現在疫情大爆發,出現「白肺」與「心肌炎」症狀的患者不斷蔓延至各個年齡層,有網友發文,家裡剛出生5天的新生兒,感染後遭醫院下病危通知書,右肺1/3出現白肺。由於中國本輪疫情中出現了大量「白肺」和「心肌炎」患者,中國網友更是創出了「白肺心肌」一詞,諷刺中共戰天鬥地的無效三年「清零」。目前,國際持續要求中共公布真實疫情數據,中國醫衛專家張文宏指出,過年期間,中國染疫比率可能高達80%,代表中國14億人口將有超過11億人染疫。
-

本土+15 桃園9例最多 境外移入+33 美國最多
2022-01-29 15:09:03今(29)日中央流行疫情指揮中心公布,國內新增15例本土個案及33例境外移入;另確診個案中無新增死亡。
-

高端獲巴拉圭EUA WHO團結試驗疫苗有望3月解盲
2022-02-15 22:36:03高端疫苗在南美洲巴拉圭執行第三期臨床試驗,完成期中分析解盲成功,中和抗體效價達對照組AZ疫苗的3.7倍,巴拉圭政府在14日正式核定高端疫苗取得緊急使用授權(EUA)。先前高端獲選為WHO團結試驗疫苗,進行第三期臨床試驗,預估在3月底、4月初會有結果,高端已準備上億劑產能,目標從國產疫苗邁向國際疫苗。
-

+37例本土 11例陰轉陽 26例不明感染源 46例境外移入
2022-02-10 15:03:47今(10)日中央流行疫情指揮中心公布,國內新增83例COVID-19確定病例,分別為37例本土個案及46例境外移入,15例為航班落地採檢陽性;另確診個案中無新增死亡。
-

中國偷偷強推第4針?!拒絕者禁出門甚至收押
2023-04-04 20:20:57近日,中共御用專家鐘南山的一番話,令人擔憂,疫情再度爆發,不是空穴來風。還有民眾透露,山東正在偷偷強推第4針疫苗,如果拒絕,被禁止出門,甚至「收押」。
-

高端疫苗技轉授權WHO 生產研發基地首曝光
2023-09-19 17:14:27台灣的國產疫苗研發實力受到國際肯定。高端COVID-19疫苗技轉授權給世界衛生組織(WHO),創下全球首例。研發十年的腸病毒71型疫苗,也已經上市。這些疫苗的生產研發基地,就在高端疫苗的新竹竹北廠區。首次對外曝光,帶您了解。
-

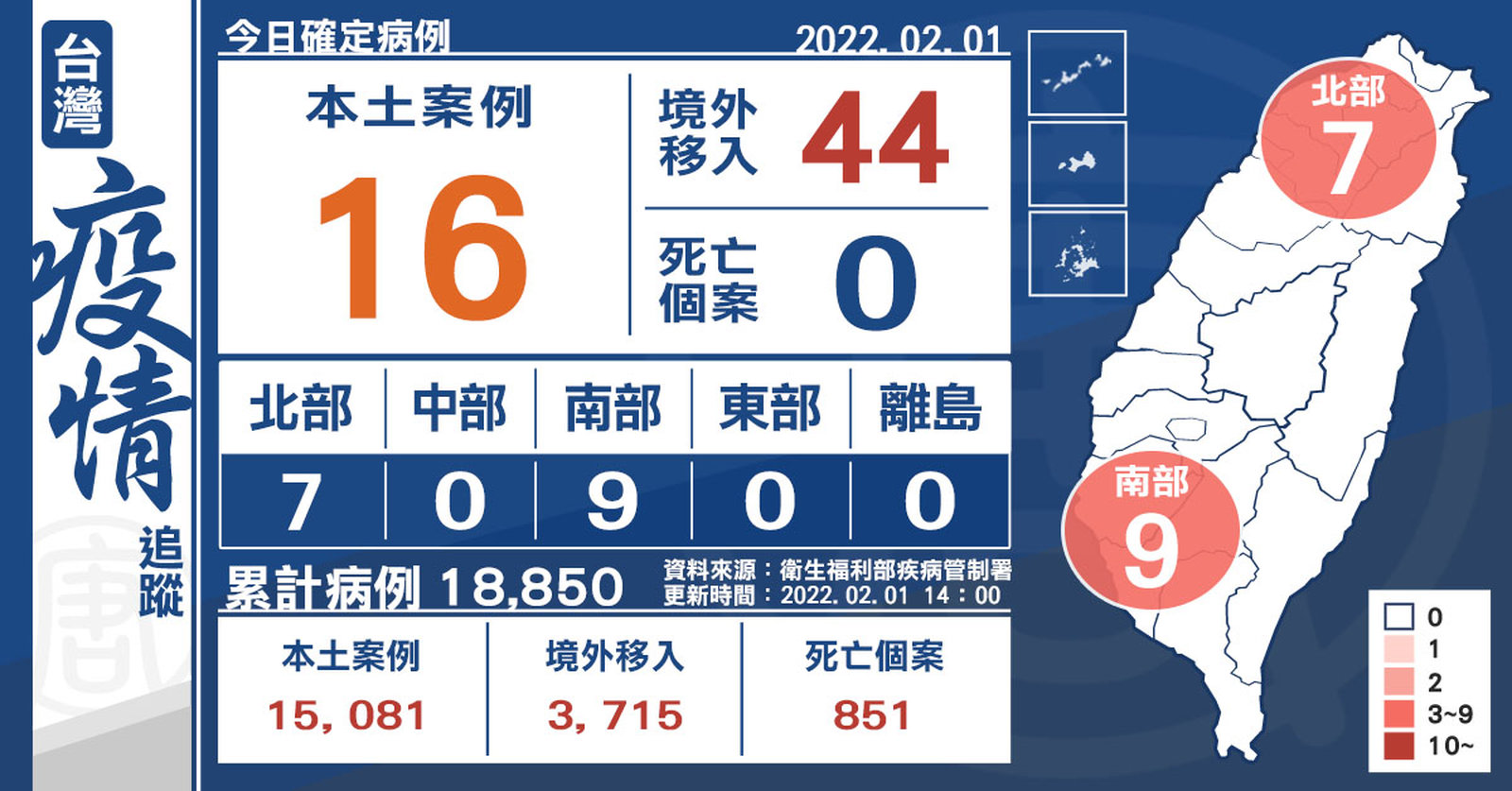
+16例本土 44例境外移入 7例落地採檢陽性
2022-02-01 15:05:48今(1)日中央流行疫情指揮中心公布,國內新增16例本土個案及44例境外移入,其中7例為航班落地採檢陽性;另確診個案中無新增死亡。
-

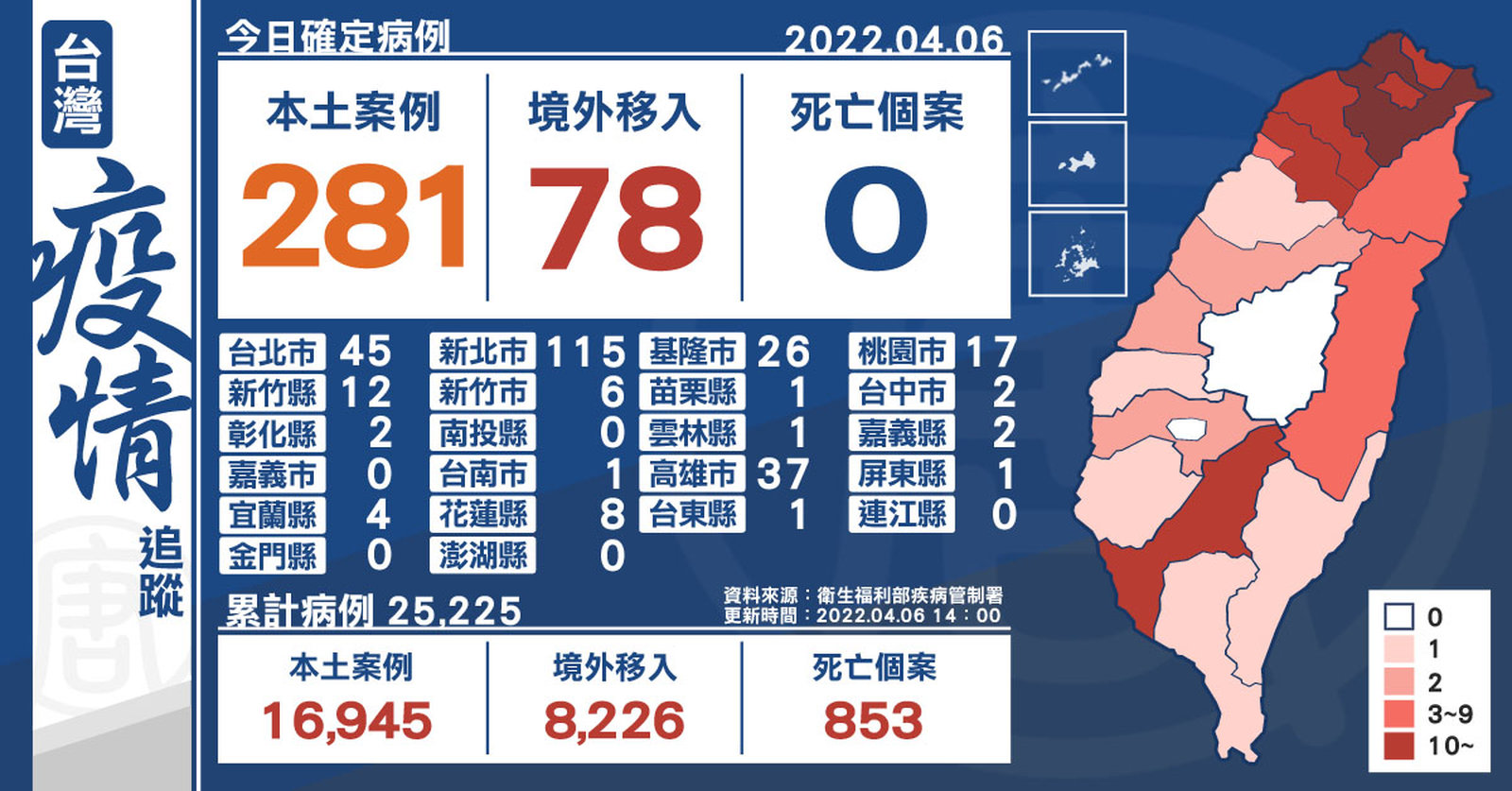
本土+281 全台17縣市確診 境外+78
2022-04-06 15:03:09中央流行疫情指揮中心今(6)日公布,國內新增359例COVID-19確定病例,分別為281例本土個案及78例境外移入,其中27例為航班落地採檢陽性;另確診個案無新增死亡。
-

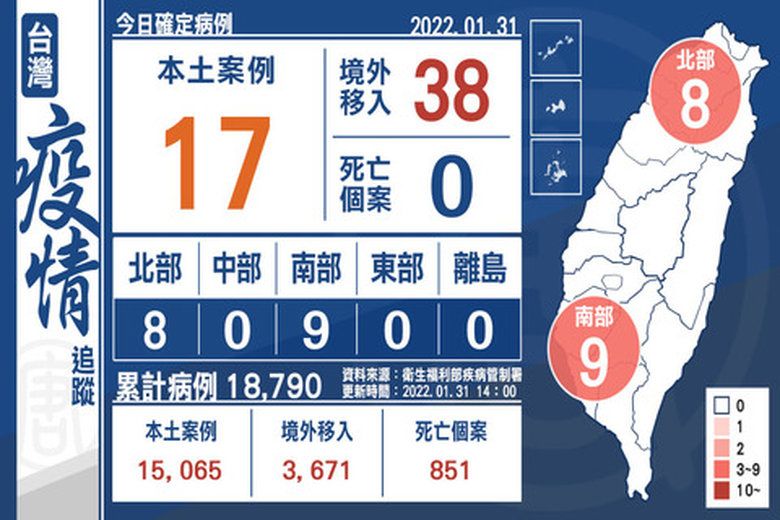
+17例本土 38例境外移入 美國最多
2022-01-31 16:33:40今(31)日中央流行疫情指揮中心公布,國內新增17例本土個案及38例境外移入(20例為航班落地採檢陽性);另確診個案中無新增死亡。